喜报!重庆华美成功备案国家医疗器械临床试验机构
近日,重庆华美整形外科医院成功备案国家医疗器械临床试验机构(GCP),标志着我院具备开展医疗器械临床试验相应的专业技术水平、组织管理能力以及伦理审查能力,是医院临床科研的全新起点,将有力提升科创研发的学术水平和技术水平,加快建设医美专科的教、学、研示范高地。
成功备案 打造科研示范平台
GCP是指Good Clinical Practice,即临床试验质量管理规范,是临床试验全过程的质量标准,包括方案设计、组织实施、监查、稽查、记录、分析总结和报告,临床试验的范围包括药物、医疗器械、诊断试剂等。
近年来,随着医美行业快速发展,医疗器械的研发与创新成为产业链条中很重要的一环。临床试验作为医疗器械研发的必经阶段,是评价其安全性和有效性最严谨的方法,也是药品监督管理部门进行审批的重要内容和关键依据。
去年6月,重庆华美全面启动GCP备案工作,依据《医疗器械临床试验机构条件和备案管理办法》、《医疗器械临床试验质量管理规范》等相关规定,组建由高级职称专家团领衔的专业研究团队,制定完善的临床试验管理制度和SOP,以保障临床试验可以顺利有序安全地开展。
历时9个多月的扎实筹备,今年3月,重庆华美完成了国家药监局医疗器械临床试验机构备案,并于3月5日顺利通过重庆市药监局组织的GCP备案后首次现场监督检查,标志着我院已具备开展医疗器械临床试验的资质与能力。
“作为一家有着26年历史的三级整形外科医院,重庆华美积极参与GCP机构建设,是为了更好地发挥人才优势与技术优势,打造集合作研发、成果转化、临床诊疗于一体的科研创新示范平台,”重庆华美医务院长向贵平介绍称。
扎实建设 促进行业高质量发展
数据显示,目前我国取得临床试验机构资质的医疗机构绝大多数为三级公立医院,占全部医院总数的比例仅1%。随着国家在医药创新领域取得明显突破,鼓励医疗机构积极开展创新医疗器械临床试验,解决临床研究资源的短缺问题,全面提升医疗科研能力。
此次重庆华美成功备案GCP,是医院实力、专科诊疗水平、临床科研能力的综合体现,接下来,我院将以此为起点,扎实推进GCP机构建设,持续引进科研和临床人才,携手上游厂商合作研发,促进成果转化,形成医美特色及专科亮点,助力行业高质量发展。
不仅如此,医院将紧跟国内外GCP管理和临床试验研究技术的最新进展,引入最前沿、最优质的临床试验资源,持续优化研发策略和试验方法,提高临床试验的安全性和可靠性,打造优质的研究平台。
“我们相信,随着国家医疗器械临床试验机构落地重庆华美,将全面提升医院的科研及诊疗水平,参与临床试验的医务人员能够接触到国内外最前沿的诊疗方案、一手的临床试验数据,这对于提升团队的学术水平,建设医美专科特色的创新研究型医院奠定了坚实基础,能够更好地服务每一位求美者,”向贵平表示。

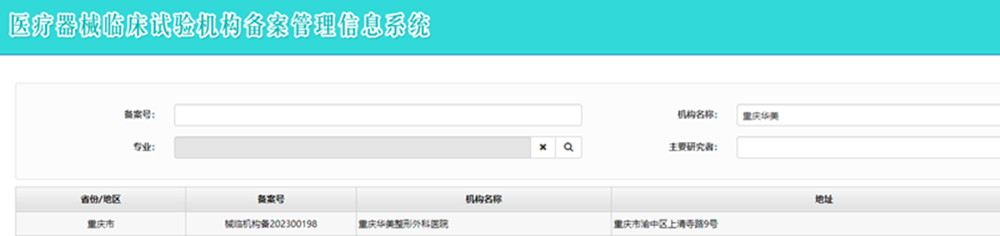
国家药品监督管理局官网备案截图
成功备案 打造科研示范平台
GCP是指Good Clinical Practice,即临床试验质量管理规范,是临床试验全过程的质量标准,包括方案设计、组织实施、监查、稽查、记录、分析总结和报告,临床试验的范围包括药物、医疗器械、诊断试剂等。
近年来,随着医美行业快速发展,医疗器械的研发与创新成为产业链条中很重要的一环。临床试验作为医疗器械研发的必经阶段,是评价其安全性和有效性最严谨的方法,也是药品监督管理部门进行审批的重要内容和关键依据。
去年6月,重庆华美全面启动GCP备案工作,依据《医疗器械临床试验机构条件和备案管理办法》、《医疗器械临床试验质量管理规范》等相关规定,组建由高级职称专家团领衔的专业研究团队,制定完善的临床试验管理制度和SOP,以保障临床试验可以顺利有序安全地开展。

重庆市药监局现场监督检查
历时9个多月的扎实筹备,今年3月,重庆华美完成了国家药监局医疗器械临床试验机构备案,并于3月5日顺利通过重庆市药监局组织的GCP备案后首次现场监督检查,标志着我院已具备开展医疗器械临床试验的资质与能力。
“作为一家有着26年历史的三级整形外科医院,重庆华美积极参与GCP机构建设,是为了更好地发挥人才优势与技术优势,打造集合作研发、成果转化、临床诊疗于一体的科研创新示范平台,”重庆华美医务院长向贵平介绍称。
扎实建设 促进行业高质量发展
数据显示,目前我国取得临床试验机构资质的医疗机构绝大多数为三级公立医院,占全部医院总数的比例仅1%。随着国家在医药创新领域取得明显突破,鼓励医疗机构积极开展创新医疗器械临床试验,解决临床研究资源的短缺问题,全面提升医疗科研能力。

重庆市药监局现场监督检查
此次重庆华美成功备案GCP,是医院实力、专科诊疗水平、临床科研能力的综合体现,接下来,我院将以此为起点,扎实推进GCP机构建设,持续引进科研和临床人才,携手上游厂商合作研发,促进成果转化,形成医美特色及专科亮点,助力行业高质量发展。
不仅如此,医院将紧跟国内外GCP管理和临床试验研究技术的最新进展,引入最前沿、最优质的临床试验资源,持续优化研发策略和试验方法,提高临床试验的安全性和可靠性,打造优质的研究平台。
“我们相信,随着国家医疗器械临床试验机构落地重庆华美,将全面提升医院的科研及诊疗水平,参与临床试验的医务人员能够接触到国内外最前沿的诊疗方案、一手的临床试验数据,这对于提升团队的学术水平,建设医美专科特色的创新研究型医院奠定了坚实基础,能够更好地服务每一位求美者,”向贵平表示。
